Энергия ионизации
Энергия ионизации
При рассмотрении модели атома водорода Бора было продемонстрированно, что поглощение света с достаточной энергией переводит электрон на более высокий энергетический уровень, а при его переходе на более низкий энергетический уровень происходит излучение света вследствие потери энергии. 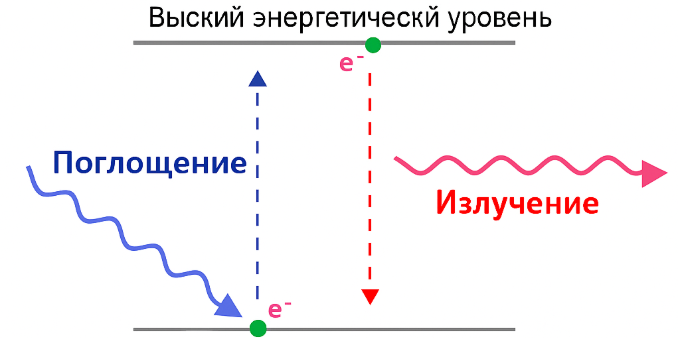
Далее, при рассмотрении фотоэлектрического эффекта было обнаружено, что если фотон, сталкивающийся с электроном, обладает энергией, превышающей энергию самого высокого энергетического уровня, электрон выбивается из атома, преодолевая все энергетические барьеры, связанные с орбитальными энергетическими уровнями:
Минимальная энергия, необходимая для удаления электрона из элемента (обычно металла), называется работой выхода (Φ) и является характеристикой каждого металла.
Понятие энергии ионизации, которое мы рассмотрим в этой статье, схоже с этим явлением, поэтому разберем, что это такое и чем оно отличается от фотоэлектрического эффекта.
Энергия ионизации
Применяя тот же принцип, что и в фотоэлектрическом эффекте, электроны также могут быть удалены из изолированных атомов в газообразном состоянии. Количество энергии, необходимое для удаления электрона из изолированного нейтрального атома в газообразном состоянии, называется энергией ионизации атома (E
i
или ЭИ).
На этом изображении атом водорода ионизирован путем удаления его единственного электрона.
Для многоэлектронных атомов существуют различные энергии ионизации в зависимости от того, какой электрон удаляется. Энергия, необходимая для удаления первого электрона с внешней валентной оболочки, является первой энергией ионизации (E
i1
), для второго электрона — E
i2
, и так далее.
Сравним энергии ионизации алюминия:
Основное наблюдение, следующее из значений энергий ионизации, заключается в том, что они увеличиваются по мере удаления последующих электронов. Первый электрон удаляется из нейтрального атома, в то время как все последующие удаляются из иона. Следовательно, можно соотнести значения энергий ионизации с зарядом иона. По мере увеличения заряда увеличивается и энергия ионизации:
Удалить электрон из иона Al
2+
труднее, чем из иона Al
1+
, что можно объяснить возрастающими электростатическими силами между катионом с более высоким зарядом и электроном.
Теперь построим график, чтобы увидеть, существуют ли другие закономерности при сравнении изменений энергий ионизации:
Обратите внимание на резкий скачок при переходе от третьей к четвертой энергии ионизации. Он значительно больше, чем разница между ЭИ₁ и ЭИ₂ или ЭИ₂ и ЭИ₃.
Итак, почему существует такая большая разница между третьей и четвертой энергиями ионизации алюминия?
Чтобы ответить на этот вопрос, необходимо рассмотреть электронную конфигурацию элемента: Al – 1s
2
2s
2
2p
6
3s
2
3p
1
:
Здесь важно то, что первые три удаляемых электрона являются валентными электронами Al, поскольку они находятся на внешнем главном энергетическом уровне (n = 3). Следует помнить, что они находятся дальше всего от ядра и, следовательно, их легче всего удалить. Другим фактором, влияющим на энергию ионизации, является экранирование электронами. В дополнение к внутренним электронам, электрон 3p
1
также экранируется 3s-электронами, в то время как последние экранируются только внутренними электронами. Таким образом, хотя удаление электрона 3p
1
все еще требует меньше энергии, чем удаление электронов 3s
2
и 3s
1
, поскольку p-подуровень имеет более высокую энергию (находится дальше от ядра), эта разница намного меньше, чем при начале удаления внутренних электронов атома.
Удаление второго 3s-электрона еще сложнее, поскольку заряд иона увеличивается, однако разница не так велика, как при переходе с главного энергетического уровня 3s на 2s. Таким образом, подводя итог этой части, можно заключить, что удалять внутренние (остовные) электроны гораздо труднее, чем валентные, из-за ионного заряда, расстояния и экранирования электрона. Это ожидаемо, поскольку известно, что именно валентные электроны участвуют в химических реакциях, так как их легче всего удалить, и, следовательно, они участвуют в образовании связей с другими элементами.
Периодические закономерности изменения энергии ионизации
Прежде всего, следует помнить, что энергия ионизации увеличивается при движении вверх по периодической таблице, потому что атомы становятся меньше, и электроны находятся ближе к ядру. Кроме того, у меньших атомов меньше электронов, что уменьшает экранирование удаляемого электрона. Рассмотрим это на примере сравнения первой энергии ионизации Li, K и Na:
Несмотря на то, что Na имеет более высокий заряд ядра, чем Li (+11 против +3), для удаления его первого электрона требуется меньше энергии. Это может показаться нелогичным, если сравнивать только заряды ядер, однако расстояние и экранирование электрона оказываются более значимыми факторами, и поскольку Na является более крупным атомом, его энергия ионизации меньше.
Таким образом, в общем случае, чем больше у атома энергетических уровней, тем меньше его энергия ионизации, поскольку они добавляют экранирование от ядра.
Вторая закономерность — это общее увеличение энергии ионизации при движении вправо по периодической таблице.
Для объяснения этого рассмотрим элементы 3-го периода периодической таблицы:
Прежде всего, следует отметить, что все элементы находятся в одном и том же периоде периодической таблицы, и, следовательно, валентные электроны находятся на одном и том же главном энергетическом уровне (n = 3). Однако отличается их заряд ядра. Атомный номер, а следовательно, и число протонов, увеличивается при движении вправо.
Общая закономерность заключается в том, что движение слева направо увеличивает энергию ионизации, хотя это не всегда верно при сравнении любых двух элементов. Например, вопреки общему тренду, Al имеет меньшую энергию ионизации, чем Mg, так же как и сера по сравнению с фосфором. Разберемся, почему у Mg более высокая энергия ионизации, чем у Al.
Причина в том, что последний валентный электрон у Al — это 3p
1
(1s
2
2s
2
2p
6
3s
2
3p
1
), в то время как у Mg — 3s
2
(1s
2
2s
2
2p
6
3s
2
). Следует помнить, что p-подуровень данного энергетического уровня находится дальше от ядра и, следовательно, электрон с него удалить легче:
Это общая закономерность, согласно которой p-электроны имеют более низкую энергию ионизации, чем s-электроны на том же энергетическом уровне.
Далее рассмотрим расхождение в энергиях ионизации серы и фосфора. S находится правее и, как ожидается, должна иметь большую энергию ионизации, но это не так. Рассмотрим электронные конфигурации этих элементов – P: (1s
2
2s
2
2p
6
3s
2
3p
3
), S – (1s
2
2s
2
2p
6
3s
2
3p
4
).
Для удаления электрона 3p
4
серы требуется немного меньше энергии (1000 кДж/моль), чем для электрона 3p
3
фосфора (1012 кДж/моль). Причиной этого являются силы отталкивания между двумя электронами на одной и той же орбитали. Следует помнить правило Хунда, которое гласит, что электроны сначала заполняют все вырожденные орбитали (равные по энергии) с параллельными спинами (обе стрелки вверх или вниз), прежде чем образовывать пары на одной орбитали. Иными словами, по возможности, электроны избегают нахождения на одной и той же орбитали.
Возвращаясь к энергии ионизации, если электрон 3p
4
стремится покинуть орбиталь (имеет более высокую энергию), на которой уже находится электрон 3p
3
, то его будет легче удалить, чем электрон 3p
3
, который находится на своей орбитали один.
Следует помнить, что меньшая энергия означает большую стабильность, и наоборот, если электрон (или что-либо еще) имеет более высокую энергию, он менее стабилен и, следовательно, его легче удалить. Таким образом, спаренные электроны на одном подуровне, как правило, удалить легче, чем неспаренные.
Обобщая закономерности изменения энергий ионизации в периодической таблице, следует помнить, что они имеют тенденцию к увеличению вверх и вправо по таблице:
